A. Biundo, V. Braunschmid, M. Pretzler, I. Kampatsikas, B. Darnhofer, R. Birner-Gruenberger, A. Rompel, D. Ribitsch & G. M. Guebitz
Commun Chem 3, 62 (2020).
自然界では、限られた数の酵素が細胞内で数百数千の反応を触媒している。酵素と生化学反応の不均衡に対処するための自然界のアプローチの一つとして、「多機能酵素」の発現がある。これらの酵素は、いくつかの異なる酵素反応を行うタンパク質である。このような多機能性は、産業応用や酵素の理解を深める上で非常に重要である。本研究では、polyphenol oxidase(PPO)のタンパク質分解機能を記述する。
tyrosinase(EC 1.14.18.1およびEC 1.10.3.1)、catechol oxidase(EC 1.10.3.1)およびaurone synthase(EC 1.21.3.6)は、タイプIII-銅タンパク質クラスに属するPPOファミリーを構成している。PPOは、あらゆる生命で普遍的に存在している。ほとんどの真核生物のPPOは、活性ドメインと遮蔽C末端ドメインを含むpro-enzymeとして発現している。植物PPOは、C末端ドメインが活性部位を覆っており、また酵素をチラコイドの内腔に誘導するN末端シグナルペプチドを含んでいる。酵素の活性化は、酸性pHで、または界面活性剤の存在下で、proteaseによるC末端ドメインの切断を介して達成される。tyrosinaseファミリーのメンバーは、cresolase活性とcatecholase活性を持っている。cresolase活性(monophenolase活性、EC 1.14.18.1)は、モノフェノールのオルトヒドロキシル化とそれに続くo-キノンへの酸化に関与している。一方、catecholase活性(diphenolase活性、EC 1.10.3.1)は、o-キノンへのo-ジフェノールの酸化に特異的である。非常に反応性の高いo-キノンは、メラニンなどの複雑なポリマーにつながるさらなる非酵素的な再配列を受けることができる。PPOのtyrosinase(cresolaseとcatecholase活性)とcatechol oxidase(catecholase活性のみ)への機構的な分割については、いまだよくわかっていない。さらに、aurone synthaseは、tyrosinaseと同様のメカニズムで、水酸化と酸化的環化によりchalconeからのauroneの生成を触媒することができる。
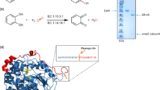
tyrosinaseは、バイオテクノロジーの多くのアプリケーションに向けて研究されている。ポリペプチドの表面に露出したチロシンをo-キノンに変換する能力のために、tyrosinaseはタンパク質の架橋するために広く使用されている。この架橋活性により、tyrosinaseは食品タンパク質の構造や食感を変化させるために、食品産業において非常に重要な存在となっている。Clostridium botulinum由来のcarboxylesterase(EstA)を適切な担体に固定化する試みにおいて、我々は最近、tyrosinaseの異常な活性を発見した。EstAを特定のtyrosinaseとインキュベートすると、EstAが完全に切断され、より大きなサブユニットとより小さなサブユニットに分離された。carboxylesterase EstAは、過去に、polybutylene adipate-co-terephthalate (PBAT)のような合成ポリエステルを加水分解することが確認されている。このcarboxylesteraseをtyrosinaseで処理すると、N末端の71個のアミノ酸を欠いたEstA(ΔEstA)が得られた。興味深いことに、ΔEstAは、可溶性および不溶性基質、例えばpolyethylene terephthalate (PET)などの基質に対して劇的に活性が改善されていることがわかった。
本研究では、いくつかのPPOのEstAに対する活性を試験した。活性は、試験した5つのPPOのうち3つに存在した。その活性は、典型的なproteaseの開裂部位として知られていないSer71とIle72の間に特異的なものであった。私たちの知る限り、この活性はPPOファミリーのメンバーで初めての報告である。


コメント