Zhang L, Li S, Liu X, Wang Z, Jiang M, Wang R, Xie L, Liu Q, Xie X, Shang D, Li M, Wei Z, Wang Y, Fan C, Luo ZQ, Shen X.
Nat Commun. 2020 Oct 23;11(1):5371.
doi: 10.1038/s41467-020-19243-5. PMID: 33097715; PMCID: PMC7584622.
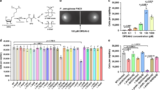
細菌のクオラムセンシング(QS)は、オートインデューサーによって媒介される細胞間コミュニケーションプロセスであり、細菌が細胞密度に依存した方法で行動を調整することを可能にしている。グラム陰性菌が産生するアシルホモセリンラクトンやグラム陽性菌が分泌するオリゴペプチドなどのオートインデューサーの大部分は、種内コミュニケーションに特化している。一方で、Autoinducer-2(AI-2)はグラム陰性菌とグラム陽性菌で広く合成され、種内および種間レベルでのコミュニケーションを媒介する能力を持っているQSシグナルである。興味深いことに、AI-2は単一のシグナル分子ではなく、4,5-dihydroxy-2,3-pentanedione(DPD)誘導体のグループであり、互いに迅速に変換される。DPDは一般的に酵素LuxSによって合成される。luxS遺伝子を欠いたいくつかの細菌では、2つの非定型AI-2合成経路が存在することが提案されている。現在までに、細菌の受容体と対応する二つのAI-2形態が同定されている。その中には、Vibrio spp.のみに存在するLuxPによって認識されるホウ素含有DPD誘導体S-2-methyl-2,3,3,4-tetrahydroxytetrahydrofuran-borate (S-THMF-borate) 、腸内細菌や他のいくつかの科のメンバーに見られるLsrB が認識する非ホウ素化R-2-methyl-2,3,3,4-tetrahydroxytetrahydrofuran (R-THMF) が含まれる。2つのAI-2形態間の急速な相互変換のために、2つの異なるタイプの受容体を有する細菌種はAI-2シグナリングを介して互いに通信することができる。
AI-2受容体LuxPとLsrBは、共にリボース結合タンパク質に相同性のあるペリプラズム結合タンパク質であるが、お互いの一次配列類似性は高くない(〜11%の同一性)。AI-2に結合したLuxPは、膜貫通センサーヒスチジンキナーゼ(HK)LuxQの活性をキナーゼからホスファターゼに変換することで、遺伝子発現を調節し、生物発光、バイオフィルム形成、病原性因子産生などの多くの密度依存性表現型を変化させる。LsrB-AI-2複合体は、細胞内にAI-2を送達するためにATP結合カセットトランスポーターシステムLsrの膜コンポーネントとして関与している。さらに、AI-2に結合したLsrBは、化学受容体Tsrのペリプラズムセンサードメインとの相互作用を介して、大腸菌の化学走性を駆動することができる。
不思議なことに、AI-2に強く反応する多数の細菌は、LuxP-またはLsrB様AI-2受容体をコードしておらず、このオートインデューサーのための他のタイプの受容体が存在する可能性を提起している。例えば、Pseudomonas aeruginosa や Enterococcus faecalis などの細菌病原体では、バイオフィルム形成や病原性因子の産生などの遺伝子発現や表現型がAI-2によって制御されている。しかし、化学プローブやバイオインフォマティクスのアプローチを用いた潜在的AI-2受容体を同定するための試みは成功しておらず、この問題を解決するためには代替的な戦略が必要である。これらのAI-2応答性細菌におけるAI-2センサーの同定ができないことは、AI-2が種内および種間コミュニケーションに参加する普遍的なシグナルとしての役割の理解を大きく妨げてきた。
ここでは、予測された化学受容体を欠くP. aeruginosa変異体のライブラリーを調べることにより、PctAとTlpQが、periplasmic double CAlcium channels and CHEmotaxis receptors (dCACHE) domainを介して、AI-2を感知していることを発見した。また、AI-2はBacillus subtilis HK KinDやRhodopseudomonas palustrisのdiguanylate cyclase(DGC)rpHK1S-Z16のdCACHEドメインによって認識され、それらの酵素活性が誘導されることも明らかにした。さらに、我々のバイオインフォマティクス解析は、AI-2を感知する性質を持つdCACHEドメインを持つシグナル伝達タンパク質が原核生物に広く分布していることを示唆しており、AI-2の検出と応答のメカニズムがこれまで認識されていなかったことを明らかにした。これらの結果は、AI-2が原核生物の間で細胞の行動を調整するためのシグナル伝達分子として広く利用されていることを裏付けるものである。


コメント